Содержание
- Актуальность проблемы
- Свойства идеального миорелаксанта
- Этапы в развитии современних миорелаксантов
- Насколько хорош неостигмин, как антагонист миорелаксантов?
- Краш-интубация (быстрая последовательная индукция)
- Заключение
- Циклодекстрины
- Хелирование, как химическое явление
- Химические свойства циклодекстринов
- Применение циклодекстринов
- Сугаммадекс
- Фармакокинетика сугаммадекса. Механизм нейтрализации стероидных миорелаксантов циклодекстранами
- Фармакодинамика сугаммадекса
- Побочные эффекты сугаммадекса
- Рекураризация при использовании сугаммадекса
- Исследования, посвященные изучению сугаммадекса
- Клиническое исследование AURORA
- Клиническое исследование SIGNAL
- Клиническое исследование SPEKTR
- Клинические исследования LIBRA, SPRING и CRYSTAL
- Sugammadex Rapidly Reverses Rocuronium Paralysis
- Заключение
- Преимущества использования сугаммадекса
Обзор публикаций «Британского журнала анестезиологии» и «Анестезия и Аналгезия» за 2006-2008 гг. Автор: Александр Мудраковский
Актуальность проблемы
Свойства идеального миорелаксанта
- Быстрое начало действия
- Быстрое или хорошо предсказуемое прекращение нейромышечной блокады
- Отсутствие (или минимальная выраженность) побочных эффектов
- Отсутствие остаточных эффектов
Этапы в развитии современних миорелаксантов
- Панкуроний, 1970-ые, лучший, чем тубокурарин
- Атракурий и векуроний. Фармакокинетические преимущества и отсутствие сердечно-сосудистых побочных эффектов
- Рокуроний, мивакурий, и цисатракурий. 1990-е. Дополнительная клиническая гибкость по сравнению с векуронием и атракурием
- Рапакурий. Быстрое начало и короткая продолжительность действия. Последняя попытка в поиске препарата способного заменить сукцинилхолин, впервые за последние 50 лет. Побочный эффект бронхоспазм – причина удаления с рынка
- Более новые миорелаксанты улучшили качество лечения пациентов (уменьшили вероятность развития остаточного паралитического действия, а также негативных сердечно-сосудистых эффектов, главным образом, из-за изменений в их фармакокинетическом профиле)
- Идеальный миорелаксант всё ещё не придуман
- Не создан идеальный агент для краш-интубации
- Рост требований: более быстрое время оборота пациентов в операционной, более тяжелые пациенты
- На данном этапе не ожидается существенного прорыва в развитии миорелаксантов Отсутствует прогресс в разработке антидотов миорелаксантов
Насколько хорош неостигмин, как антагонист миорелаксантов?
- Клинико-фармакологические свойства хорошо изучены и известны
- Низкая стоимость
- Не оказывают влияния на связывание миорелаксантов с рецепторами ацетилхолина
- Короткая продолжительность действия — возможна рекураризация
- М-холиномиметик, чем и обусловливаются все побочные эффекты: брадикардия, гиперсаливация, бронхоспазм, усиление перистальтики
- Тошнота и рвота могут представлять определенную проблему
Краш-интубация (быстрая последовательная индукция)
- Неостигмин не является подходящим препаратом для полного реверса эффекта сукцинилхолина после краш-интубации (неподходящий механизм действия)
- Сукцинилхолин — препарат короткого действия, однако у 3-4 % населения дефицит плазменной холинэстеразы!
Заключение
- Современные антогонисты миорелаксантов слишком далеки от идеальных
Циклодекстрины
Хелирование, как химическое явление
- Связывание молекул гостя в молекулу хозяина силами Ван-дер-Ваальса, гидрофобными и электростатическими взаимодействиями
- Принцип «ключ — замок»
- Потенциально обратимый процесс
- Не вызывает изменения в химической структуре
Химические свойства циклодекстринов
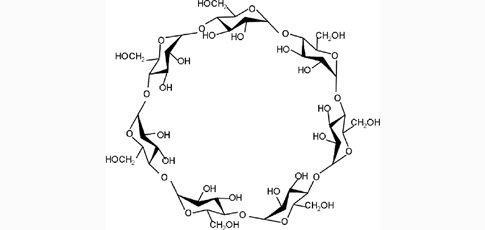
- Побочные продукты деградации крахмала
- Представляют собой группу цилиндрических олигосахаридов с гидрофобным ядром и гидрофильной оболочкой, содержащих 6, 7 или 8 молекул декстрозы
- Молекулярная масса 973, 1135, 1297, соответственно
- Хорошо исследованы
- Могут быть модифицированы – боковая цепь молекулы глюкозы или кольцо молекулы глюкозы
- Высоко растворимы в воде
- Биологически не активны, хорошо переносятся
Применение циклодекстринов
- Используются для улучшения фармакокинетических и фармакодинамических свойств лекарств
- Применяются в качестве переносчиков других медикаментов при назальном и трансдермальном путях введения
- С давних пор используются для улучшения растворимости других лекарственных препаратов. Улучшают проницаемость через кожу таких лекарств, как стероиды, препараты для химиотерапии, пропофол, назальный мидазолам
- Делают возможным ректальный путь введения лекарств (бензодиазепины, НПВС, опиаты)
- Вызываемое местное раздражение минимально
- Используются для создания препаратов продленного действия и с замедленным высвобождением лекарственной субстанции
Сугаммадекс
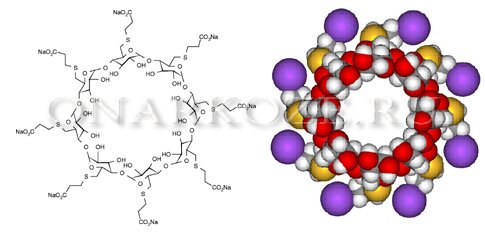
Фармакокинетика сугаммадекса. Механизм нейтрализации стероидных миорелаксантов циклодекстранами
- Гамма-циклодекстрин
- Липофильный центр
- Гидрофобная внешняя оболочка
- Силы Ван-дер-Ваальса
- Реакция происходит в плазме, а не в нейромышечном синапсе – связывание сугаммадекса с миорелаксантом приводит к снижению градиента концентрации между плазмой и синапсами
- Комплексы свободно фильтруются в почках (клиренс = 120-150 мл/минуты)
- Диссоциация комплекса не происходит — хелирование не является обратимым процессом?
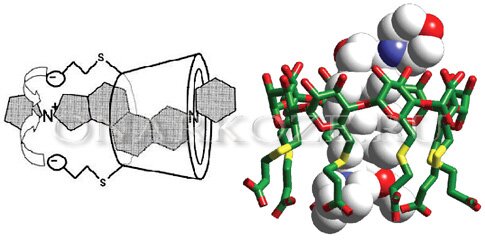
Фармакодинамика сугаммадекса
- Может противодействовать эффектам только стероидных миорелаксантов
- Не оказывает влияния на бензоквинолоны
- Эффект не обратим – рекураризация не возможна?
- Доза 8 мг/кг вызывает полную реверсию блока за 3 минуты
- Может приводить к хелированию других стеройдов (альдостерон, кортизол, половые гормоны и немного наркотиков)
- Отсутствие мускариновых побочных эффектов
- Увеличивает интервал QT
- Преходящая гипотензия после введения больших доз
- Комплекс выводится из организма почечной фильтрацией, не приводя к развитию ОПН, ХПН
Побочные эффекты сугаммадекса
- Наиболее часто встречающаяся неблагоприятная реакция, о которой обычно сообщают, это металлический или горький прикус во рту
- Также нередки сообщения об осложнениях анестезии, обусловленных восстановлением нейромышечного проведения, включающих движения тела, конечностей, кашель во время анестезиологических процедур или хирургии
- Есть несколько сообщений об аллергических реакциях (эритематозная сыпь)
Рекураризация при использовании сугаммадекса
- Возвращение нейромышечного блока может произойти тогда, когда антидот (сугаммадекс) выводится из организма быстрее, чем происходит разрушение и выводение миорелаксанта. Это явления возможно только при введении неадекватно низкой дозы сугаммадекса
- Сугаммадекс нейтрализует также и другие аминостероидные миорелаксанты, к примеру, векуроний и панкуроний
- Нейтрализация векурония происходит достаточно эффективно, так как в естественных условиях присутствует меньшее количество молекул векурония необходимых для эквивалентной блокады. Векуроний является примерно в семь раз более мощным миорелаксантом, чем рокуроний, поэтому для нейромышечной блокады требуется примерно в семь раз меньше молекул сугаммадекса
- Сугаммадекс связывается в соотношении 1:1, поэтому он полностью блокирует векуроний
Исследования, посвященные изучению сугаммадекса
Клиническое исследование AURORA
- Международное рандомизированное мультицентровое исследование было проведено в 13 европейских центрах параллельно. В исследовании участвовали 198 взрослых пациентов, перенесших оперативное вмешательство
- Рокуроний вводился в стандартной дозе, достаточной для проведения интубации трахеи. В дальнейшем, при необходимости, для поддержания нейромышечной блокады вводились дополнительные дозы препарата
- При умеренном блоке (чему соответствует появление T2, по данным TOF) пациентами вводили или сугаммадекс или неостигмин с гликопирролатом
- Среднее время востановления нейромышечного проведения к значению TOF 0.9 произошло через 1,4 минуты в сугаммадекс-группе, по сравнению с 17.6 минутами в группе неостигмин/гликопирролат
- Побочные эффекты наблюдались у 34 пациентов (14 в группе сугаммадекса, 20 в группе неостигмина)
- Большинство побочных эффектов имели умеренную выраженность
- Наиболее частые побочные эффекты (> 4 %), встречающиеся после введения сугаммадекса, включает: сухость во рту, тошноту, рвоту, озноб, транзиторную гипертонию
- Использование неостигмина чаще всего (> 4 %) ассоциировалось с такими побочными явлениями, как пролонгированная нейромышечная блокада, сухостью во рту, тошнота, альбуминурия
Клиническое исследование SIGNAL
- Включало взрослых пациентов, переносящих операцию
- Для интубации трахеи вводилась стандартная доза рокурония (0,6 мг/кг). Для поддержание миорелаксации (по мере необходимости) вводились дополнительные дозы препарата (0,15 мг/кг)
- При появление T1-2 (по данным TOF) пациентам вводился сугаммадекс или неостигмин с гликопирролатом
- Среднее время восстановления нейромышечной проводимости (TOF 0,9) составило 2,7 минуты в группе сугаммадекса и 49,0 минут в группе неостигмина/гликопирролата
Клиническое исследование SPEKTR
- 110 пациентов, подвергшихся требующему непродолжительной миорелаксации плановому оперативному вмешательству, были рандомизированы на две группы. Пациентам первой группы вводился рокуроний в дозе 1,2 мг/кг, затем через 3 минуты сугаммадекс в дозе 16 мг/кг. Вторая группа пациентов получила сукцинилхолин в дозе 1 мг/кг
- Среднее время восстановления нейромышечной проводимости (TOF 90%), отмеченное от начала введения миорелаксантов, составило: в группе рокуроний/сугаммадекс — 6,2 минуты, в группе сукцинилхолина – 10,9 минут. Причём время восстановления мышечного тонуса от начала введения сугаммадекса было около 2,9 минут
- Наиболее частыми побочными эффектами, отмечаемыми при введении рокуроний/сугаммадекса и сукцинилхолина, были боль в месте введения (57% против 48%, соответственно) и тошнота (29% против 37 %, соответственно). В обеих группах не было отмечено никаких серьёзных осложнений, а также явления восстановления нейро-мышечного блока (рекураризации)
Клинические исследования LIBRA, SPRING и CRYSTAL
- Сугаммадекс зарекомендовал себя высокоэффективным препаратом с хорошей переносимость при его использовании у детей и пациентов, имеющих умеренные или выраженные нарушения почечной функции
- В этих исследованиях наиболее распространенными (> 4 %) побочными эффектами, связанными с применением сугаммадекса, были диарея и повышение уровня д-глюкозаминидазы
- В конечном счёте, сугаммадекс продемонстрировал способность полной реверсии вызванного рокуронием нейромышечного блока в течение 3 минут
Sugammadex Rapidly Reverses Rocuronium Paralysis
Ron M. Walls, MD, FRCPC,FAAEM. Journal Watch Emergency Medicine August 8, 2008
- Европейское мультицентровое рандомизированное исследование, в котором приняло участие 168 пациентов
- Оценка способности сугаммадекса вызывать нейтрализацию более высоких доз рокурония, используемых для быстрой последовательной индукции
- Плановая анестезия, доза рокурония 1,0 или 1,2 мг/кг
- Через 3 или 15 минут после применения рокурония вводился или сугаммадекс в одной из пяти дозировок (2, 4, 8, 12,16 мг/кг) или плацебо
- Проводилось непрерывное мониторирование TOF до достижения значения ответа 90%, и в течение не менее 30 минут после введения сугаммадекса
- При введении высоких доз сугаммадекса (16 мг/кг) через 3 или 15 минут после применения 1,0 мг/кг рокурония среднее время восстановления нейромышечного проведения составляло 1,6 и 0,9 минут, соответственно
- В случае применения рокурония в дозе 1,2 мг/кг соответствующее время восстановления мышечного тонуса наблюдалось через 1,3 и 1,9 минут, соответственно
- У пациентов получивших плацебо среднее время восстановления нейромышечного проведения колебалось от 91 до 124 минут
- У 22 из 157 пациентов (14%), которым вводился сугаммадекс, развились тошнота, рвота
- У 11 пациентов группы сугаммадекса наблюдалось развитие серьезной побочной реакции в виде удлинения интервала QT. Исследователи полагают, что достоверная связь между этим феноменом и фактом применения сугаммадекса может быть установлена только в одном случае
Заключение
- Необходимо использовать большую дозу сугаммадекса, когда рокуроний применяется в дозе необходимой для проведения краш-индукции (1,0 мг/кг). В рутинной практике сугаммадекс используется в дозировке (0,6 мг/кг)
- Введение сугаммадекса в большей дозе достаточно эффективно и не связано с какими-либо очевидными отрицательными побочными эффектами
- Возможность выполнения полного реверса нейромышечного блока за время менее 2 минут означает, что рокуроний может достаточно безопасно использоваться для проведения методики быстрой последовательной индукции (краш-индукции)
Преимущества использования сугаммадекса
- Безопасность использования миорелаксантов у пациентов с заболеваниями печени или почек
- Отсутствие характерных неостигмину и гликопирролату побочных эффектов
- Отсутствие эффекта рекураризации
- Отсутствие потребности мониторинга нейромышечного блока?
- Значительное уменьшение времени восстановления нейро-мышечного проведения
- Полное изменение философии быстрой последовательной индукции из-за отсутствия риска апное
- Отсутствие проблем связанных с применением сукцинилхолина (ожоги, паралич, глазная хирургия, злокачественная гипертермия)
- Изменение подхода к анестезии при миастении, нейромышечных заболеваниях, болезнях печени и почек